Bactéries intestinales et Saccharomyces boulardii
Les probiotiques sont des micro-organismes vivants qui ont un effet bénéfique sur la santé (intestinale) de leur hôte. Il s’agit principalement de bactéries, comme des lactobacilles et des bifidobactéries. Mais il existe également un micro-organisme non bactérien classé comme probiotique : la Saccharomyces boulardii. Ce type de levure est étudié depuis plusieurs dizaines d’années en raison de ses propriétés spécifiques et est de plus en plus reconnu comme un probiotique prometteur. [1]
S. boulardii a été découverte en 1920 par le microbiologiste français Henri Boulard au cours d’une visite en Indochine. Le microbiologiste avait remarqué que les populations locales qui buvaient une décoction préparée à partir de l’écorce de litchis et de mangoustans ne développaient aucun symptôme du choléra. Il a pris des échantillons, a isolé la levure et lui a donné le nom de Saccharomyces boulardii. En tant que levure, la S. boulardii se distingue des probiotiques bactériens par sa taille, la composition de sa paroi cellulaire, sa résistance aux antibiotiques et ses propriétés mé- taboliques. [1]
Les organismes vivants sont classés selon leur genre, leur espèce et leur souche. S. boulardii est une souche unique qui appartient à l’espèce Saccharomyces cerevisiae, comme la levure de boulanger. En dépit d’une parenté génomique de plus de 99 % avec les souches S. cerevisiae non probiotiques, on note des différences importantes dans son action sur la santé humaine. [2]
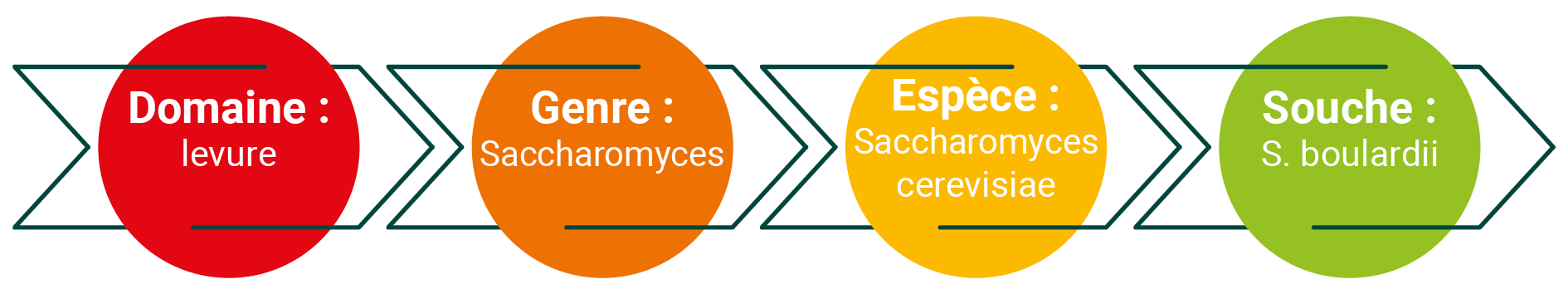 Figure 1. classification S. boulardii.
Figure 1. classification S. boulardii.
Des propriétés uniques en cas de dysbioses
S. boulardii présente plusieurs propriétés qui en font un probiotique unique et précieux (voir figure 2) : [3-5]
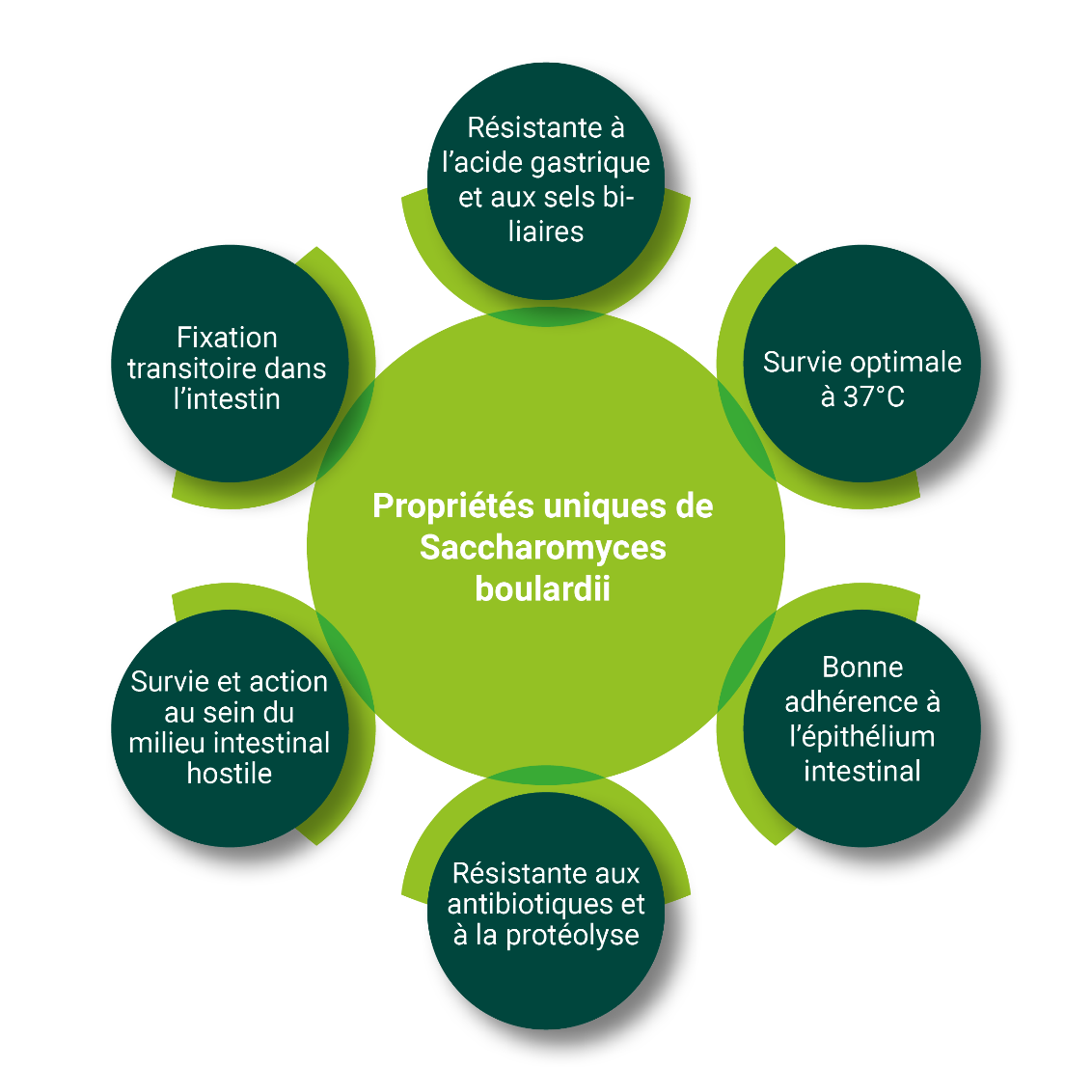 Figure 2 : Propriétés uniques de S. boulardii.
Figure 2 : Propriétés uniques de S. boulardii.
- Sous forme lyophilisée, S. boulardii résiste à l’acide gastrique et aux acides biliaires. Elle franchit donc aisément l’estomac et l’intestin grêle. Pratique, puisque S. boulardii a surtout un effet dans le colon.
- S. boulardii survit de manière optimale à 37°C. C’est ainsi une des rares levures qui s’épanouit à la température du corps humain.
- S. boulardii résiste aux antibiotiques. La levure peut donc survivre et être efficace pendant une cure d’antibiotiques, alors que de nombreux autres micro-organismes sont détruits.
- S. boulardii est résistante à la protéolyse, la dégradation par des enzymes qui dégradent les protéines (protéases). Cette propriété contribue à préserver la viabilité de la levure même quand elle est exposée à l’environnement acide de l’estomac et à l’environnement enzymatique des intestins.
- S. boulardii survit et agit dans l’environnement hostile du système intestinal. Les souches de levures ont la capacité de s’auto-agréger, de s’agglomérer et à se regrouper. C’est une réaction de survie qui leur permet de mieux résister à des conditions environnementales défavorables. Elle offre à la cellule de levure un avantage compétitif par rap- port à d’autres micro-organismes. Outre sa capacité à s’auto-agréger, S. boulardii dispose également d’une surface cellulaire hydrophobe (imperméable à l’eau). Auto-agrégation et hydrophobie de la surface cellulaire permettent toutes deux une adhérence optimale à l’épithélium intestinal. Elle occupe ainsi les sites de fixation des bactéries pathogènes ; celles-ci ne pourront donc pas se adhérer à l’épithélium intestinal et seront éliminées plus rapidement.
- Contrairement aux probiotiques bactériens, S. boulardii ne se fixe pas de manière permanente dans les intestins. Après absorption, elle ne reste présente que temporairement dans le corps ; trois à cinq jours après administration, la cellule a disparu. S. boulardii remplit sa fonction lors de son passage dans le système digestif.
Quels sont les principaux mécanisme d’action de Saccharomyces boulardii ?
S. boulardii possède plusieurs mécanismes d’action qui peuvent être répartis en trois principales actions : [3]
- Action dans le lumière intestinale
- Action trophique / impact sur la production d’enzymes digestives
- Action anti-inflammatoire sur les muqueuses

Les principales applications actuelles d’une cure de Saccharomyces boulardii
L’efficacité de S. boulardii comme probiotique thérapeutique est prouvée dans plusieurs pathologies. Les principales applications sont décrites ci-dessous.
Diarrhées
S. boulardii est efficace dans différents types de diarrhées. C’est notamment le probiotique le plus efficace pour prévenir et traiter des diarrhées associées aux antibiotiques et une infection à Clostridioides difficile (ICD). [7] Clostridium diffi- cile est une des principales causes de diarrhées associées aux antibiotiques. Un des mécanismes qui mènent à ce type de diarrhée pendant la prise d’antibiotique est la réduction de la conversion microbienne d’acides biliaires primaires en acides biliaires secondaires. Les acides biliaires primaires favorisent la croissance et la prolifération de C. difficile, alors que les acides biliaires secondaires réduisent leur croissance et/ou leur prolifération. S. boulardii prévient la perturbation du métabolisme des acides biliaires pendant une thérapie antibiotique et constitue ainsi un mécanisme de protection contre une diarrhée post antibiotique. [2]
En outre, S. boulardii est la seule souche probiotique qui présente une efficacité significative dans la prévention de la diarrhée du voyageur. S. boulardii est plus efficace dans la réduction de l’incidence de la diarrhée du voyageur que des souches bactériennes comme Lactobacillus rhamnosus ou Lactobacillus acidophilus. [2]
S. boulardii affiche également une efficacité éprouvée dans le traitement de diarrhées aiguës et la prévention de diarrhées liées à une alimentation entérale par sonde. [5]
La diarrhée et d’autres pathologies gastro-intestinales comme les nausées peuvent également être la conséquence du traitement d’une infection à Helicobacter pylori. Helicobacter pylori est une bactérie à Gram négatif qui constitue une des principales causes de gastrite chronique, du cancer du côlon et de l’intestin grêle, et du lymphome du tissu lymphoïde associé aux muqueuses. L’utilisation de S. boulardii est efficace dans la réduction des effets secondaires d’un traitement de l’Helicobacter pylori et constitue donc un complément judicieux au plan de traitement. De plus, S. boulardii ajoute dans une certaine mesure un effet inhibiteur à la bactérie Helicobacter pylori. Dans des cas modérés, l’administration de S. boulardii permet même de se passer de traitements médicamenteux. [2,8]
Maladies Inflammatoires Chroniques de l‘Intestin (MICI)
Les maladies inflammatoires de l’intestin sont caractérisées par des inflammations qui affectent l’intégrité de la barrière épithéliale. Les protéines des jonctions serrées sont essentielles à la préservation de la fonction barrière épithéliale et au contrôle de la perméabilité de l’intestin. S. boulardii protège l’expression de protéines des jonctions serrées, la zona-occludens-1 et l’occludine. [2]
Outre les jonctions serrées, d’autres liaisons sont importantes dans la régulation de la perméabilité intestinale : les jonctions adhérentes. Les jonctions adhérentes se trouvent immédiatement sous les jonctions serrées et garantissent une liaison adhérente dynamique entre les cellules épithéliales. Dans l’épithélium de l’intestin, la glycoprotéine transmembranaire cadhérine E est un élément important des jonctions adhérentes. On constate une expression réduite et/ou une dislocation de la cadhérine E chez les patients souffrant de MICI. S. boulardii rétablit l’intégrité de la barrière intestinale en régulant le recyclage de la cadhérine E. [2,9]
Les propriétés anti-inflammatoires S. boulardii et le fait que son administration accroisse la présence d’acides gras à chaîne courte (AGCC) sont également importants dans la prévention et le traitement des MICI. S. boulardii réduit le ni- veau de TNF-α et d’IL-8, des cytokines qui jouent un rôle important dans la pathogenèse des MICI. Les AGCC améliorent l’intégrité de la paroi intestinale. [2, 10]
Syndrome du côlon irritable (SCI)
Les recherches menées sur la S. boulardii et le SCI montrent une réduction des symptômes gastro-intestinaux et par conséquent une amélioration de la qualité de vie. [2,5]
Prolifération de Candida
L’infection à C. albicans se développe souvent après un traitement antibiotique. Elle est plus grave et plus fréquente chez les personnes immunodéprimées. En raison de la résistance accrue des souches de C. albicans aux antimycotiques, des stratégies thérapeutiques complémentaires sont nécessaires. L’administration de S. boulardii est appropriée à la fois pour traiter et prévenir l’infection à C. albicans. L’acide caprique sécrété par S. boulardii freine en effet la croissance des filaments mycéliens, qui assurent l’adhérence et la formation du biofilm de C. albicans. [2]
Marqueurs métaboliques
L’administration de S. boulardii a une influence bénéfique sur plusieurs marqueurs métaboliques. Ainsi, on attribue un rôle intéressant à S. boulardii dans la prise en charge du surpoids et de l’obésité. La présence de ces pathologies est – en autre – liée au rapport entre les deux principales souches bactériennes : les firmicutes et les bactéroïdètes. Le microbiome des personnes en surpoids est plus riche en firmicutes et moins riche en bactéroïdètes. Les firmicutes sont plus efficaces au moment d’extraire de l’énergie des aliments et facilitent ainsi une absorption plus efficace des calories et la prise de poids qui s’ensuit. [11] L’administration de S. boulardii a ici un effet modulateur : elle réduit la concentration en firmicutes et accroît la concentration en bactéroïdètes. [4]
L’obésité fait partie des maladies chroniques dites de civilisation. En raison de son action anti-inflammatoire, S. boulardii a également un effet bénéfique sur ce type de pathologie. [4] Mais d’autres marqueurs sont également influencés positive- ment par S. boulardii. Ainsi, une étude sur des humains dans laquelle des participants obèses se sont vu administrer 500 mg S. boulardii avec 1000 UI SOD pendant 60 jours a permis de constater une baisse significative de l’IMC et de la masse graisseuse, mais aussi une baisse de l’insuline, de l’indice HOMA et de l’acide urique. [12]
L’influence positive sur la présence d’AGCC est également bénéfique pour les marqueurs métaboliques. Outre leur action sur l’intégrité de la barrière intestinale, ces AGCC améliorent en effet le métabolisme du glucose et des graisses et régu- lent le système immunitaire, la réaction inflammatoire et la pression artérielle. [10]
Enfin, l’administration de S. boulardii a pour effet de réguler le profil de cholestérol et réduit la concentration totale en triglycérides. Cela provient d’une part du fait que la paroi cellulaire de S. boulardii contient du β-glucane, des mannopro- téines et de la chitine, dont on sait qu’elles favorisent l’absorption de cholestérol. D’autre part, cette action a également un lien indirect avec le rôle de S. boulardii dans la modulation du microbiome intestinal et la régulation de la production de cytokines pro-inflammatoires. [4]
Avertissement général
Saccharomyces boulardii est déconseillé pour les personnes, porteuses d’un cathéter veineux central ou allergiques aux levures et moisissures.
Conclusion sur l’intérêt de Saccharomyces boulardii et références
S. boulardii est une levure thérapeutique active classée comme probiotique non bactérien. Cette levure présente des propriétés prometteuses et efficaces pour des troubles et pathologies variés, comme différentes formes de diarrhées, de maladies inflammatoires chroniques de l’intestin, le syndrome du côlon irritable, la prolifération de candida et l’amélioration de plusieurs marqueurs métaboliques. Contrairement aux probiotiques bactériens, l’action de S. boulardii n’est pas altérée par les antibiotiques et elle conserve par conséquent ses propriétés pro- biotiques quand elle est administrée avec des médicaments antibiotiques.
Références
1. Czerucka D, Rampal P. Diversity of Saccharomyces boulardii CNCM I-745 mechanisms of action against intestinal infections. World J Gastroenterol. 2019. DOI: 10.3748/wjg.v25.i18.2188.
2. Kaźmierczak-Siedlecka K, Ruszkowski J, Fic M, et al. Saccharomyces boulardii CNCM I-745: A Non-bacterial Microorganism Used as Probiotic Agent in Supporting Treatment of Selected Diseases. Curr Microbiol. 2020. DOI: 10.1007/s00284-020-02053-9.
3. Gopalan S, Ganapathy S, Mitra M, et al. Unique Proper- ties of Yeast Probiotic Saccharomyces boulardii CNCM I-745: A Narrative Review. Cureus. 2023. DOI: 10.7759/ cureus.46314.
4. Egea MB, Oliveira Filho JG, Lemes AC. Investigating the Efficacy of Saccharomyces boulardii in Metabolic Syn- drome Treatment: A Narrative Review of What Is Known So Far. Int J Mol Sci. 2023. DOI: 10.3390/ijms241512015.
5. McFarland LV. Systematic review and meta-analysis of Saccharomyces boulardii in adult patients. World J Gastroenterol. 2010. DOI: 10.3748/wjg.v16.i18.2202.
6. Moré MI, Vandenplas Y. Saccharomyces boulardiiCNCM I-745 Improves Intestinal Enzyme Function: A Trophic Effects Review. Clin Med Insights Gastroenterol. 2018. DOI: 10.1177/1179552217752679.
7. Kelesidis T, Pothoulakis C. Efficacy and safety of the probiotic Saccharomyces boulardii for the prevention and therapy of gastrointestinal disorders. Therap Adv Gastroenterol. 2012. DOI: 10.1177/1756283X11428502.
8. Qu P, Liu X, Xia X, et al. Saccharomyces boulardii Allows Partial Patients to Avoid Reusing Bismuth Quadruple for Helicobacter pylori Rescue Therapy: A Single-Center Randomized Controlled Study. Front Cell Infect Micro- biol. 2022. DOI: 10.3389/fcimb.2022.903002.
9. Terciolo C, Dobric A, Ouaissi M, et al. Saccharomyces boulardii CNCM I-745 Restores intestinal Barrier Integrity by Regulation of E-cadherin Recycling. J Crohns Colitis. 2017. DOI: 10.1093/ecco-jcc/jjx030.
10. Nogal A, Valdes AM, Menni C. The role of short-chain fat- ty acids in the interplay between gut microbiota and diet in cardio-metabolic health. Gut Microbes. 2021. DOI: 10.1 080/19490976.2021.1897212.
11. Magne F, Gotteland M, Gauthier L, et al. The Firmicutes/ Bacteroidetes Ratio: A Relevant Marker of Gut Dysbio- sis in Obese Patients? Nutrients. 2020. DOI: 10.3390/ nu12051474.
12. Rondanelli M, Miraglia N, Putignano P, et al. Effects of 60-Day Saccharomyces boulardii and Superoxide Dis- mutase Supplementation on Body Composition, Hun- ger Sensation, Pro/Antioxidant Ratio, Inflammation and Hormonal Lipo-Metabolic Biomarkers in Obese Adults: A Double-Blind, Placebo-Controlled Trial. Nutrients. 2021. DOI: 10.3390/nu13082512.
Saccharomyces boulardii : une levure probiotique prometteuse aux propriétés uniques
Les probiotiques sont des micro-organismes vivants qui ont un effet bénéfique sur la santé (intestinale) de leur hôte. Il s’agit principalement de bactéries, comme des lactobacilles et des bifidobactéries. Mais il existe également un micro-organisme non bactérien classé comme probiotique : la Saccharomyces boulardii. Ce type de levure est étudié depuis plusieurs dizaines d’années en raison de ses propriétés spécifiques et est de plus en plus reconnu comme un probiotique prometteur. [1]
S. boulardii a été découverte en 1920 par le microbiologiste français Henri Boulard au cours d’une visite en Indochine. Le microbiologiste avait remarqué que les populations locales qui buvaient une décoction préparée à partir de l’écorce de litchis et de mangoustans ne développaient aucun symptôme du choléra. Il a pris des échantillons, a isolé la levure et lui a donné le nom de Saccharomyces boulardii. En tant que levure, la S. boulardii se distingue des probiotiques bactériens par sa taille, la composition de sa paroi cellulaire, sa résistance aux antibiotiques et ses propriétés mé- taboliques. [1]
Les organismes vivants sont classés selon leur genre, leur espèce et leur souche. S. boulardii est une souche unique qui appartient à l’espèce Saccharomyces cerevisiae, comme la levure de boulanger. En dépit d’une parenté génomique de plus de 99 % avec les souches S. cerevisiae non probiotiques, on note des différences importantes dans son action sur la santé humaine. [2]
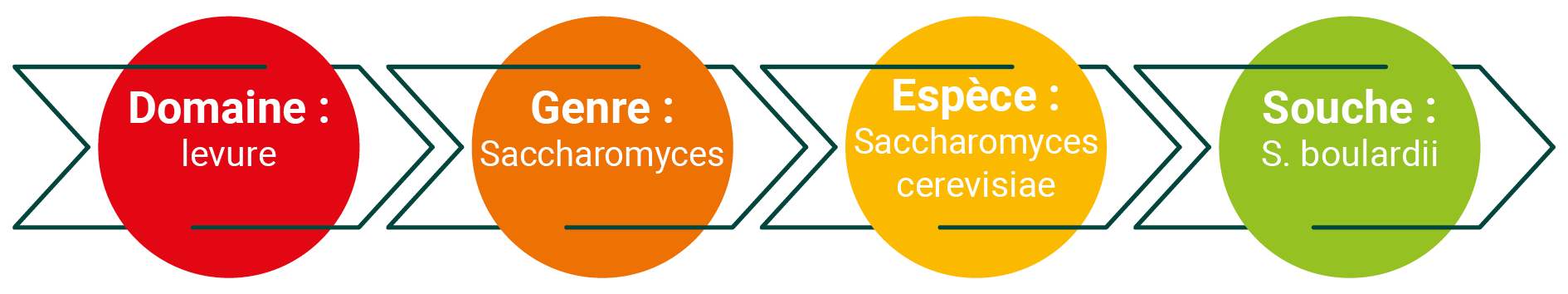 Figure 1. classification S. boulardii.
Figure 1. classification S. boulardii.
Propriétés uniques
S. boulardii présente plusieurs propriétés qui en font un probiotique unique et précieux (voir figure 2) : [3-5]
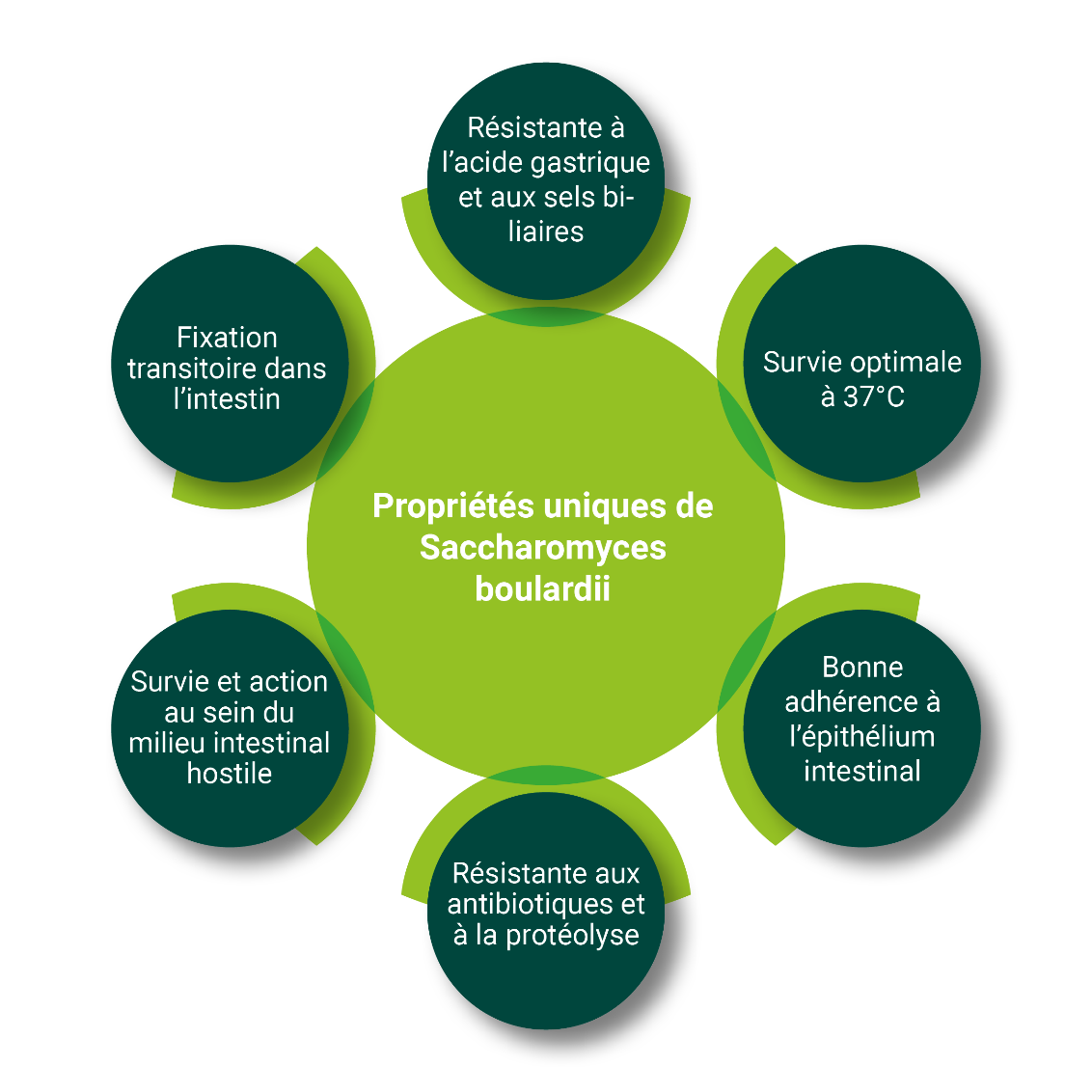 Figure 2 : Propriétés uniques de S. boulardii.
Figure 2 : Propriétés uniques de S. boulardii.
- Sous forme lyophilisée, S. boulardii résiste à l’acide gastrique et aux acides biliaires. Elle franchit donc aisément l’estomac et l’intestin grêle. Pratique, puisque S. boulardii a surtout un effet dans le colon.
- S. boulardii survit de manière optimale à 37°C. C’est ainsi une des rares levures qui s’épanouit à la température du corps humain.
- S. boulardii résiste aux antibiotiques. La levure peut donc survivre et être efficace pendant une cure d’antibiotiques, alors que de nombreux autres micro-organismes sont détruits.
- S. boulardii est résistante à la protéolyse, la dégradation par des enzymes qui dégradent les protéines (protéases). Cette propriété contribue à préserver la viabilité de la levure même quand elle est exposée à l’environnement acide de l’estomac et à l’environnement enzymatique des intestins.
- S. boulardii survit et agit dans l’environnement hostile du système intestinal. Les souches de levures ont la capacité de s’auto-agréger, de s’agglomérer et à se regrouper. C’est une réaction de survie qui leur permet de mieux résister à des conditions environnementales défavorables. Elle offre à la cellule de levure un avantage compétitif par rap- port à d’autres micro-organismes. Outre sa capacité à s’auto-agréger, S. boulardii dispose également d’une surface cellulaire hydrophobe (imperméable à l’eau). Auto-agrégation et hydrophobie de la surface cellulaire permettent toutes deux une adhérence optimale à l’épithélium intestinal. Elle occupe ainsi les sites de fixation des bactéries pathogènes ; celles-ci ne pourront donc pas se adhérer à l’épithélium intestinal et seront éliminées plus rapidement.
- Contrairement aux probiotiques bactériens, S. boulardii ne se fixe pas de manière permanente dans les intestins. Après absorption, elle ne reste présente que temporairement dans le corps ; trois à cinq jours après administration, la cellule a disparu. S. boulardii remplit sa fonction lors de son passage dans le système digestif.
Mécanisme d’action
S. boulardii possède plusieurs mécanismes d’action qui peuvent être répartis en trois principales actions : [3]
- Action dans le lumière intestinale
- Action trophique / impact sur la production d’enzymes digestives
- Action anti-inflammatoire sur les muqueuses

Principales applications
L’efficacité de S. boulardii comme probiotique thérapeutique est prouvée dans plusieurs pathologies. Les principales applications sont décrites ci-dessous.
Diarrhée
S. boulardii est efficace dans différents types de diarrhées. C’est notamment le probiotique le plus efficace pour prévenir et traiter des diarrhées associées aux antibiotiques et une infection à Clostridioides difficile (ICD). [7] Clostridium diffi- cile est une des principales causes de diarrhées associées aux antibiotiques. Un des mécanismes qui mènent à ce type de diarrhée pendant la prise d’antibiotique est la réduction de la conversion microbienne d’acides biliaires primaires en acides biliaires secondaires. Les acides biliaires primaires favorisent la croissance et la prolifération de C. difficile, alors que les acides biliaires secondaires réduisent leur croissance et/ou leur prolifération. S. boulardii prévient la perturbation du métabolisme des acides biliaires pendant une thérapie antibiotique et constitue ainsi un mécanisme de protection contre une diarrhée post antibiotique. [2]
En outre, S. boulardii est la seule souche probiotique qui présente une efficacité significative dans la prévention de la diarrhée du voyageur. S. boulardii est plus efficace dans la réduction de l’incidence de la diarrhée du voyageur que des souches bactériennes comme Lactobacillus rhamnosus ou Lactobacillus acidophilus. [2]
S. boulardii affiche également une efficacité éprouvée dans le traitement de diarrhées aiguës et la prévention de diarrhées liées à une alimentation entérale par sonde. [5]
La diarrhée et d’autres pathologies gastro-intestinales comme les nausées peuvent également être la conséquence du traitement d’une infection à Helicobacter pylori. Helicobacter pylori est une bactérie à Gram négatif qui constitue une des principales causes de gastrite chronique, du cancer du côlon et de l’intestin grêle, et du lymphome du tissu lymphoïde associé aux muqueuses. L’utilisation de S. boulardii est efficace dans la réduction des effets secondaires d’un traitement de l’Helicobacter pylori et constitue donc un complément judicieux au plan de traitement. De plus, S. boulardii ajoute dans une certaine mesure un effet inhibiteur à la bactérie Helicobacter pylori. Dans des cas modérés, l’administration de S. boulardii permet même de se passer de traitements médicamenteux. [2,8]
Maladies Inflammatoires Chroniques de l‘Intestin (MICI)
Les maladies inflammatoires de l’intestin sont caractérisées par des inflammations qui affectent l’intégrité de la barrière épithéliale. Les protéines des jonctions serrées sont essentielles à la préservation de la fonction barrière épithéliale et au contrôle de la perméabilité de l’intestin. S. boulardii protège l’expression de protéines des jonctions serrées, la zona-occludens-1 et l’occludine. [2]
Outre les jonctions serrées, d’autres liaisons sont importantes dans la régulation de la perméabilité intestinale : les jonctions adhérentes. Les jonctions adhérentes se trouvent immédiatement sous les jonctions serrées et garantissent une liaison adhérente dynamique entre les cellules épithéliales. Dans l’épithélium de l’intestin, la glycoprotéine transmembranaire cadhérine E est un élément important des jonctions adhérentes. On constate une expression réduite et/ou une dislocation de la cadhérine E chez les patients souffrant de MICI. S. boulardii rétablit l’intégrité de la barrière intestinale en régulant le recyclage de la cadhérine E. [2,9]
Les propriétés anti-inflammatoires S. boulardii et le fait que son administration accroisse la présence d’acides gras à chaîne courte (AGCC) sont également importants dans la prévention et le traitement des MICI. S. boulardii réduit le ni- veau de TNF-α et d’IL-8, des cytokines qui jouent un rôle important dans la pathogenèse des MICI. Les AGCC améliorent l’intégrité de la paroi intestinale. [2, 10]
Syndrome du côlon irritable (SCI)
Les recherches menées sur la S. boulardii et le SCI montrent une réduction des symptômes gastro-intestinaux et par conséquent une amélioration de la qualité de vie. [2,5]
Prolifération de Candida
L’infection à C. albicans se développe souvent après un traitement antibiotique. Elle est plus grave et plus fréquente chez les personnes immunodéprimées. En raison de la résistance accrue des souches de C. albicans aux antimycotiques, des stratégies thérapeutiques complémentaires sont nécessaires. L’administration de S. boulardii est appropriée à la fois pour traiter et prévenir l’infection à C. albicans. L’acide caprique sécrété par S. boulardii freine en effet la croissance des filaments mycéliens, qui assurent l’adhérence et la formation du biofilm de C. albicans. [2]
Marqueurs métaboliques
L’administration de S. boulardii a une influence bénéfique sur plusieurs marqueurs métaboliques. Ainsi, on attribue un rôle intéressant à S. boulardii dans la prise en charge du surpoids et de l’obésité. La présence de ces pathologies est – en autre – liée au rapport entre les deux principales souches bactériennes : les firmicutes et les bactéroïdètes. Le microbiome des personnes en surpoids est plus riche en firmicutes et moins riche en bactéroïdètes. Les firmicutes sont plus efficaces au moment d’extraire de l’énergie des aliments et facilitent ainsi une absorption plus efficace des calories et la prise de poids qui s’ensuit. [11] L’administration de S. boulardii a ici un effet modulateur : elle réduit la concentration en firmicutes et accroît la concentration en bactéroïdètes. [4]
L’obésité fait partie des maladies chroniques dites de civilisation. En raison de son action anti-inflammatoire, S. boulardii a également un effet bénéfique sur ce type de pathologie. [4] Mais d’autres marqueurs sont également influencés positive- ment par S. boulardii. Ainsi, une étude sur des humains dans laquelle des participants obèses se sont vu administrer 500 mg S. boulardii avec 1000 UI SOD pendant 60 jours a permis de constater une baisse significative de l’IMC et de la masse graisseuse, mais aussi une baisse de l’insuline, de l’indice HOMA et de l’acide urique. [12]
L’influence positive sur la présence d’AGCC est également bénéfique pour les marqueurs métaboliques. Outre leur action sur l’intégrité de la barrière intestinale, ces AGCC améliorent en effet le métabolisme du glucose et des graisses et régu- lent le système immunitaire, la réaction inflammatoire et la pression artérielle. [10]
Enfin, l’administration de S. boulardii a pour effet de réguler le profil de cholestérol et réduit la concentration totale en triglycérides. Cela provient d’une part du fait que la paroi cellulaire de S. boulardii contient du β-glucane, des mannopro- téines et de la chitine, dont on sait qu’elles favorisent l’absorption de cholestérol. D’autre part, cette action a également un lien indirect avec le rôle de S. boulardii dans la modulation du microbiome intestinal et la régulation de la production de cytokines pro-inflammatoires. [4]
Avertissement général
Saccharomyces boulardii est déconseillé pour les personnes, porteuses d’un cathéter veineux central ou allergiques aux levures et moisissures.
Conclusion
S. boulardii est une levure thérapeutique active classée comme probiotique non bactérien. Cette levure présente des propriétés prometteuses et efficaces pour des troubles et pathologies variés, comme différentes formes de diarrhées, de maladies inflammatoires chroniques de l’intestin, le syndrome du côlon irritable, la prolifération de candida et l’amélioration de plusieurs marqueurs métaboliques. Contrairement aux probiotiques bactériens, l’action de S. boulardii n’est pas altérée par les antibiotiques et elle conserve par conséquent ses propriétés pro- biotiques quand elle est administrée avec des médicaments antibiotiques.
Références
1. Czerucka D, Rampal P. Diversity of Saccharomyces boulardii CNCM I-745 mechanisms of action against intestinal infections. World J Gastroenterol. 2019. DOI: 10.3748/wjg.v25.i18.2188.
2. Kaźmierczak-Siedlecka K, Ruszkowski J, Fic M, et al. Saccharomyces boulardii CNCM I-745: A Non-bacterial Microorganism Used as Probiotic Agent in Supporting Treatment of Selected Diseases. Curr Microbiol. 2020. DOI: 10.1007/s00284-020-02053-9.
3. Gopalan S, Ganapathy S, Mitra M, et al. Unique Proper- ties of Yeast Probiotic Saccharomyces boulardii CNCM I-745: A Narrative Review. Cureus. 2023. DOI: 10.7759/ cureus.46314.
4. Egea MB, Oliveira Filho JG, Lemes AC. Investigating the Efficacy of Saccharomyces boulardii in Metabolic Syn- drome Treatment: A Narrative Review of What Is Known So Far. Int J Mol Sci. 2023. DOI: 10.3390/ijms241512015.
5. McFarland LV. Systematic review and meta-analysis of Saccharomyces boulardii in adult patients. World J Gastroenterol. 2010. DOI: 10.3748/wjg.v16.i18.2202.
6. Moré MI, Vandenplas Y. Saccharomyces boulardiiCNCM I-745 Improves Intestinal Enzyme Function: A Trophic Effects Review. Clin Med Insights Gastroenterol. 2018. DOI: 10.1177/1179552217752679.
7. Kelesidis T, Pothoulakis C. Efficacy and safety of the probiotic Saccharomyces boulardii for the prevention and therapy of gastrointestinal disorders. Therap Adv Gastroenterol. 2012. DOI: 10.1177/1756283X11428502.
8. Qu P, Liu X, Xia X, et al. Saccharomyces boulardii Allows Partial Patients to Avoid Reusing Bismuth Quadruple for Helicobacter pylori Rescue Therapy: A Single-Center Randomized Controlled Study. Front Cell Infect Micro- biol. 2022. DOI: 10.3389/fcimb.2022.903002.
9. Terciolo C, Dobric A, Ouaissi M, et al. Saccharomyces boulardii CNCM I-745 Restores intestinal Barrier Integrity by Regulation of E-cadherin Recycling. J Crohns Colitis. 2017. DOI: 10.1093/ecco-jcc/jjx030.
10. Nogal A, Valdes AM, Menni C. The role of short-chain fat- ty acids in the interplay between gut microbiota and diet in cardio-metabolic health. Gut Microbes. 2021. DOI: 10.1 080/19490976.2021.1897212.
11. Magne F, Gotteland M, Gauthier L, et al. The Firmicutes/ Bacteroidetes Ratio: A Relevant Marker of Gut Dysbio- sis in Obese Patients? Nutrients. 2020. DOI: 10.3390/ nu12051474.
12. Rondanelli M, Miraglia N, Putignano P, et al. Effects of 60-Day Saccharomyces boulardii and Superoxide Dis- mutase Supplementation on Body Composition, Hun- ger Sensation, Pro/Antioxidant Ratio, Inflammation and Hormonal Lipo-Metabolic Biomarkers in Obese Adults: A Double-Blind, Placebo-Controlled Trial. Nutrients. 2021. DOI: 10.3390/nu13082512.
Bonjour
Après lecture de cet article pour lequel je vous remercie
Je me demande quel produit acheter contenant du s boulardi pour un sibo avec constipation.
Je vous remercie. Sincèrement.
Roselyne Verbeke
Probablement le plus simple est de rajouter s boulardii (ultralevure) mais en effet le laboratoire HYGIE LAB propose le complexe de probiotiques ENTERO BIOTE particulièrement intéressant en cas de SIBO (dès la fin des boites d’antimicrobiens) car ça va continuer à assainir l’écosystème intestinal, surtout si on rajoute le fucosyllactose de loin le meilleur du marché qui FUCOBIOTE 100% (même labo) puisque ça va améliorer nettement l’adhérence des probiotiques
Selon les recherches du labo, juste après ENTERO BIOTE il est recommandé de faire une bonne cure de leur complexe BIFIDO BIOTE, puis éventuellement LACTO BIOTE
J’en profite pour rappeler que la cause immédiate et n°1 du SIBO est
1) un manque de vitalité nerveuse des muqeuses digestives dès l’estomac (atteinte du complexe moteur migrant)
2) manque de sommeil réparateur
3) manque de muscles digestifs (parfois en lien avec un manque de protéines animales)
4) présence de perturbateurs endocriniens qui créé des perturbations de la thyroide en particulier et souvent un trop plein d’oestrogènes
Bonjour, je prends la levure s boulardii du labo LESCUYER et j’en suis satisfaite.
Je vois que vous ne mentionnez pas ce labo. Pourquoi ??
J’ai découvert dans un article que s boulardii améliorait les personnes ayant des « parasites » comme blastocystis (de mémoire) . Je pense avoir récolté ce pb dans les toilettes du TGV !
que pensez vous de ma réflexion ? merci. Cordialement.
VOTRE ARTICLE EST TRES INSTRUCTIF MERCI
Bonjour, oui le labo Lescuyer est un très bon labo leur S. boulardii est la même que les autres labo : les milieux scientifiques ne citent en général jamais les labos (heureusement) et communiquent uniquement sur les nutriments ou les technologies sur lesquels ils travaillent.
Bonjour,
J’aimerais savoir.
J’ai une thyroïdite d’Hashimoto.
Je prends du S. Boulardii depuis plus d’un mois et je me retrouve plutôt constipée.
Est ce normal ?
Merci pour votre article
bonjour
non ça peut arriver car ce n’est pas forcément ce que demande prioritairement votre microbiote. S. boulardi sera bénéfique plutot en cas de candidose et en cas d’antibiothérapies. En fait pour savoir dont a besoin prioritairement votre microbiote il est recommandé de prévoir une analyse de la composition du microbiote afin d’envisager une action permettant de rétablir graduellement son équilibre.
Précisons qu’étant donné que les probiotiques ont très faible capacité d’adhérence au microbiote il existe de nouvelles approches (entre autres avec le fucosyllactose, le butyrate et certaines fibres prébiotiques) permettant d’améliorer cette adhérence.
J’en profite pour signaler que l’autre grand coupable de la baisse immunitaire et donc le déclenchement des pathologies auto-immunes, ce sont les pollutions, et probablement même ces pollutions seraient encore plus impliquées dans la genèse de ces pathologies et des cancers, que les déséquilibres du microbiote (ou plutot des microbiotes).
La baisse immunitaire serait donc extrêmement multifactoriel, et engloble même la notion de mémoires transgénérationnelles et d’équilibres énergiétiques et émotionelles dont on parle de plus en plus dans les neurosciences.
Ainsi agir sur la thyroïdite d’hashimoto avec des nutriments du microbiote c’est agir intelligemment mais c’est agir sur une infime partie de la causalité.
Est ce que vous conseillez de prendre aussi des levures intestinales comme Saccharomyces Boulardii et si oui à quelle dose par jour ?
je l’ai trouver sur cette pharmacie en ligne
merci pour votre réponse
En fait pour le SIBO (après le protocole permettant d’assainir le grêle) je recommande en particulier cette souche : Saccharomyces boulardii CNCM-3799
Le dosage est de 10 milliards par jour (optimal : 5 milliards matin et soir